前言?:血管靶向治疗是晚期NSCLC内科治疗中的重要治疗手段,以安罗替尼为代表的小分子药物和以Avastin为代表的大分子药物均已经在临床应用多年。随着Avastin的专利到期,众多生物类似药逐渐进入临床,为抗血管生成治疗提供了全新的治疗选择。
研究背景
2020年,肺癌新发病例和死亡病例分别为220万和180万,其中1/3的病例出现在中国,80~85%的晚期肺癌患者为非小细胞肺癌。在过去20年,众多新的治疗策略为晚期非小细胞肺癌的一线治疗带来新的选择,其中,抗血管生成治疗是非常重要的治疗策略。贝伐单抗是第一款被用于临床的抗血管生成药物,于2004年、2005年和2015年分别在美国、欧洲和中国获批与化疗联合应用治疗晚期非鳞非小细胞肺癌患者。而进入免疫治疗时代后,IMpower-150研究发现,贝伐单抗联合阿替利珠单抗及含铂双药化疗可以给患者带来更好的获益。为了提高贝伐单抗的可及性,研发贝伐单抗生物类似药非常重要,LY01008是一款Avastin的生物类似药,前期研究发现,该产品与Avastin在药代动力学和毒理学方面具有一致性。这项III期临床研究旨在比较LY01008联合含铂双药化疗与Avastin联合含铂双药化疗一线治疗晚期非小细胞肺癌的疗效及安全性,
本研究纳入全国67家研究中心的经过组织病理学或细胞病理学确认的转移性或局部晚期非小细胞肺癌患者,患者年龄18~75周岁且PS评分0~1分,具有一个可测量病灶。既往接受过化疗、复合有小细胞成分、侵犯大血管以及有症状的脑转移患者不允许入组。研究记录EGFR基因突变状态但并不作为强制入排标准。研究基于年龄、性别及EGFR基因突变状态进行分层。符合入组标准的患者按照1:1的比例,随机分为LY01008或Avastin组。化疗方案中,卡铂AUC=6,紫杉醇剂量为175 mg/m2,治疗周期数为4~6周期,随后给予LY01008或Avastin维持治疗,直至疾病进展或出现不可耐受毒性反应。本研究主要终点为ORR,次要研究终点包括DCR、DOR、PFS、OS及安全性。研究每6周进行一次疗效评估。该研究假设两组均有42%的患者可获得客观缓解,若LY01008 90%可信区间位于0.75~1.33之间,则认为达到预设的等效性边界。
从2017年12月至2019年5月,共计649例患者接受随机化。LY01008组和Avastin组分别入组324例和325例患者,其中,分别有293例和296例患者组成符合方案集分析人群。两组分别有85.3%和86.1%的患者完成4周期治疗,分别有43.7%和43.9%的患者完成6周期治疗。
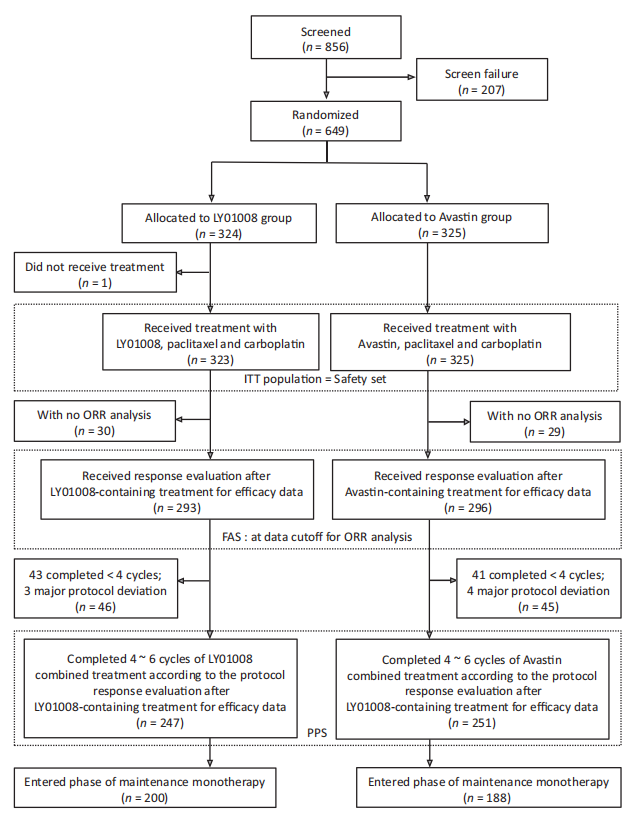
图1 研究的入组流程
疗效:两组ORR分别为56%和58.8%,ORR风险比为0.91,90%的可信区间为0.80~1.04,落在预设的等效性边界内(0.75~1.33);DCR分别为95.6%和93.6%,DCR风险比为1.03,90%可信区间为0.99~1.06(图2)。

图2 ORR的亚组分析
在符合方案集中,全组患者中位随访时间13.6个月,中位DOR分别为5.62个月和5.72个月,P=0.508;中位PFS分别为7.16个月和7.10个月,P=0.812;两组中位OS分别为24.38个月和22.97个月,P=0.479,1年OS率分别为79.4%和78.1%(图3)。

图3 两组患者的中位DOR(A)、PFS(B)及OS(C)
安全性:两组分别有99.1%和98.5%的患者出现任何级别的治疗相关不良反应,其中 LY 01008和Avastin相关的3度及以上不良反应发生率分别为37.8%和41.8%,另有70.9%和77.2%的3度及以上不良反应考虑和化疗有关(图4)。

图4 两组部分安全性数据
在中国晚期非鳞、非小细胞肺癌患者中,LY01008与Avstin具有相似的疗效及安全性。因此LY01008与卡铂和紫杉醇联合应用,应当成为这部分患者的一线治疗选择。
参考文献:Shi Y et al. Cancer Commun. 2021 Jun 29. doi: 10.1002/cac2.12179.





 京公网安备 11010502033352号
京公网安备 11010502033352号