编者按:目前临床已有多个ALK抑制剂用于ALK阳性NSCLC的治疗,为加强广大医师对ALK阳性NSCLC治疗的经验交流,更好的服务临床,《瞭望塔台》组织了“tALK show:点亮ALK阳性NSCLC之光”系列巡讲活动。
2020年4月27日第二场直播活动主题为“克唑替尼进展后,该何去何从?”,活动由江苏省肿瘤医院史美祺教授主持,华中科技大学协和医院董晓荣教授、西安交通大学第一附属医院姚煜教授、河北医科大学第四医院史健教授、福建省肿瘤医院林根教授等分别授课并对该议题展开了热烈的讨论。
董晓荣教授:《一代ALK抑制剂序贯二代ALK抑制剂治疗提供长期生存》
1. NCCN指南推荐:一代ALK抑制剂进展后更换二代
最新的NCCN治疗指南提出:一代ALK抑制剂克唑替尼进展后,对于无症状或出现症状(例如脑转移、系统性进展)的患者,均推荐更换二代ALK抑制剂包括阿来替尼、布加替尼、塞瑞替尼治疗。
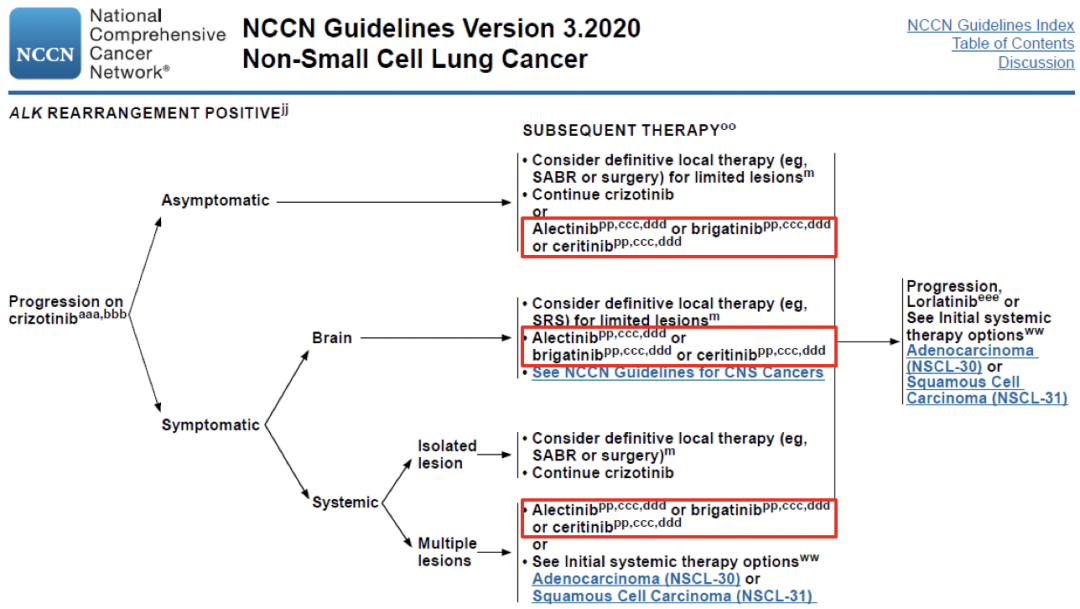 图1. NCCN-NSCLC指南(2020.3)
图1. NCCN-NSCLC指南(2020.3)
2. 一代ALK抑制剂序贯二代ALK抑制剂对生存获益最大
PROFILE 1014研究显示,一代ALK抑制剂序贯ALK抑制剂的mOS还未达到,而序贯化疗的mOS仅20.8个月。
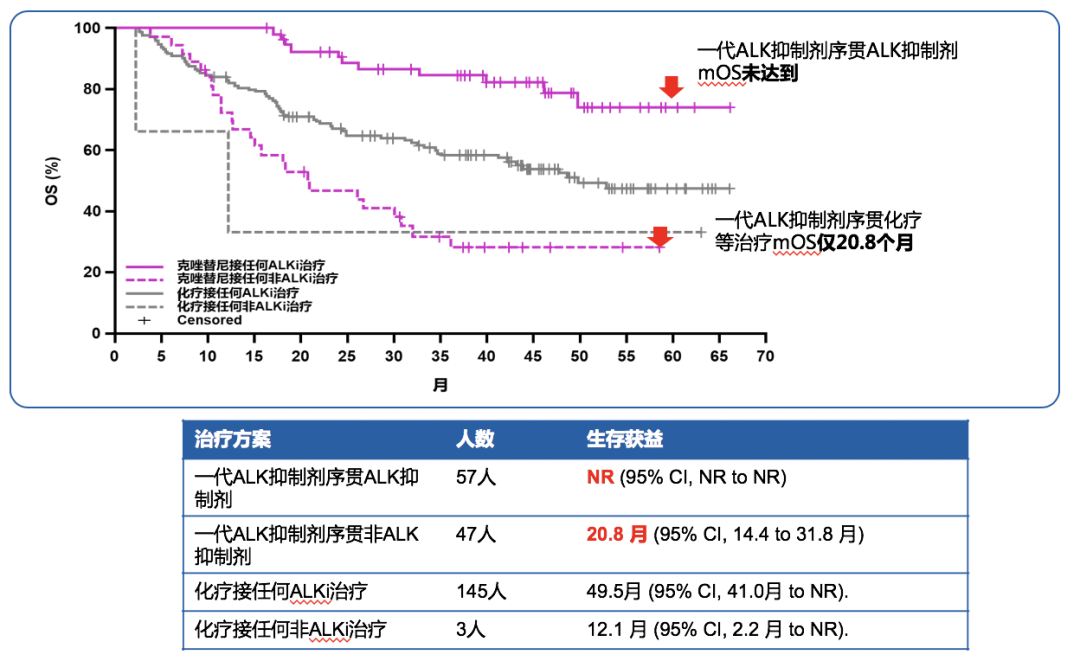 图2. PROFILE 1014研究结果来源:J Clin Oncol. 2018;36(22):2251-2258.
图2. PROFILE 1014研究结果来源:J Clin Oncol. 2018;36(22):2251-2258.
IFCT-1302 CLINALK真实世界研究分析了318例确诊ALK阳性的晚期NSCLC,从疾病确诊到开始一代ALK抑制剂治疗的平均时间为13.9个月, 此前患者大多接受铂类或紫衫类化疗。分析结果显示,克唑替尼对mOS贡献为16.6个月。这一数据与PROFILE 1014研究中,一代ALK抑制剂序贯化疗等治疗带来的中位OS获益(20.8个月)类似,而克唑替尼序贯塞瑞替尼等二代ALK抑制剂mOS可达89.6个月,其中75%患者首选塞瑞替尼。
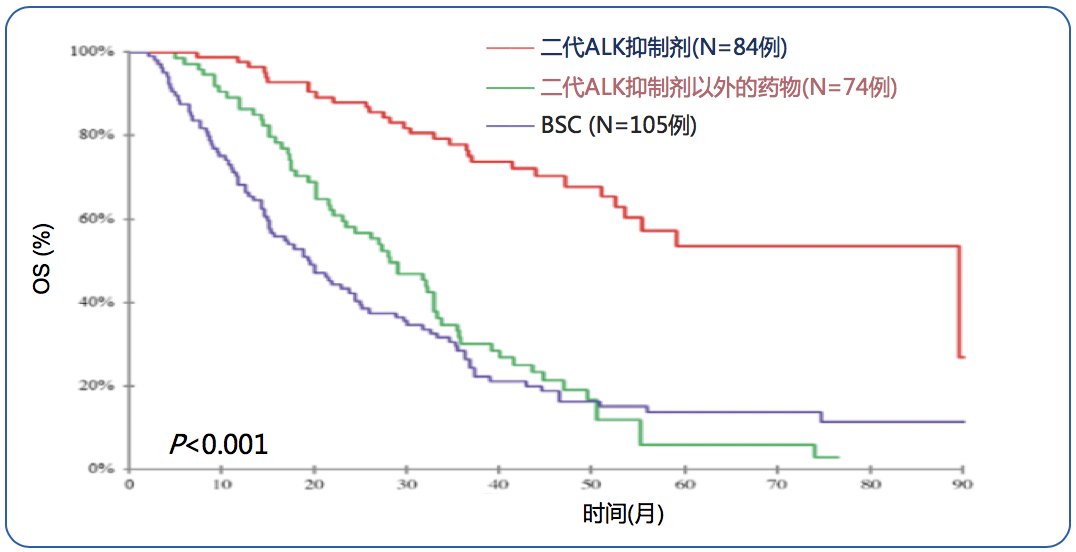 图3. IFCT-1302 CLINALK研究结果来源:Oncotarget. 2017;8(13):21903-21917.
图3. IFCT-1302 CLINALK研究结果来源:Oncotarget. 2017;8(13):21903-21917.
?
1. 一代ALK抑制剂进展后,如何选择下一步治疗?一代ALK抑制剂进展,什么时候予以换药?
史健教授:ALK阳性NSCLC患者应用一代ALK抑制剂进展后,根据原发病灶、转移病灶的具体情况分析,分为快速进展、缓慢进展和局部进展。快速进展患者应再活检基因检测,缓慢进展建议继续使用原先的ALK抑制剂,局部病灶进展可在原用药基础上加用局部治疗。
林根教授:一代ALK抑制剂进展后可选择二代ALK抑制剂,但二代ALK抑制剂目前尚无头对头比较研究结果。若条件允许,进展后首选NGS检测,若无条件行NGS检测,根据目前得到的证据,一代ALK抑制剂进展后二次突变G1202R突变占并不高,因此可根据药物经济学、性价比原则选用任意一个二代ALK抑制剂。
在目前已有二代ALK抑制剂可选的情况下,一代进展后的换药时点可根据NGS检测耐药机制为依据更换用药。若为寡进展,则选择续用一代药物加局部处理。
董晓荣教授:耐药后的选择可从精准医学、临床医学两方面考虑。通过NGS检测明确耐药机制、选择后续用药,也可根据临床情况,分为寡进展、缓慢进展、爆发进展,对寡进展患者续用一代药物加用局部治疗。参考EGFR-TKI奥西替尼的ARUA3研究,根据RECIST评价标准,出现任意部位的进展即可寻找精确靶点进行后续治疗。
1. 总体疗效
二代ALK抑制剂的临床研究中,因基线不同、评价体系不同,无法进行疗效的直接比较。比较塞瑞替尼ASCEND-1和阿来替尼(NP28673+NP28761)研究亚组分析的结果,两者ORR(65.4% vs. 58.5%)、mPFS(8.2 vs. 8.4个月)相似。
2. 颅内控制
有症状进展期脑转移和无症状稳定期脑转移的患者相比,有症状的患者预后OS(4 vs. 7.5个月)及疗效DCR(80% vs. 40%)都更差,在症状出现之前发现脑转移并予以干预,能够改善患者的预后。二代ALK抑制剂一线治疗临床研究中有关颅内疗效的结果对比可从以下三方面深入:
1)脑转移患者基线差异: ASCEND-4研究入组脑转移患者中60%为有症状进展期脑转移,ALEX入组的为稳定期(≥2周)无症状脑转移患者,两研究无法直接比较。
2)脑膜转移:对于棘手的脑膜转移,塞瑞替尼在ASCEND-7研究中给出了目前唯一的有效数据结果。该研究脑膜转移患者中,不仅纳入了ECOG2分,还有78%的患者伴有脑转移,既往接受过包括放疗、手术、化疗等多线治疗,其中88.9%的患者既往接受过克唑替尼治疗。研究结果显示,对于脑膜转移患者,塞瑞替尼治疗mPFS达5.2个月,OS达7.2个月。因此,对于一开始伴有或在治疗过程出现脑膜转移的患者,可考虑将塞瑞替尼作为治疗首选。
3)放疗对疗效的影响:ASCEND-1研究显示,放疗不影响塞瑞替尼颅内疗效,而NP28761和NP28673研究荟萃分析显示,阿来替尼治疗曾接受放疗和未接受放疗的CORR分别为35.8%和58.5%,疗效降低40%。
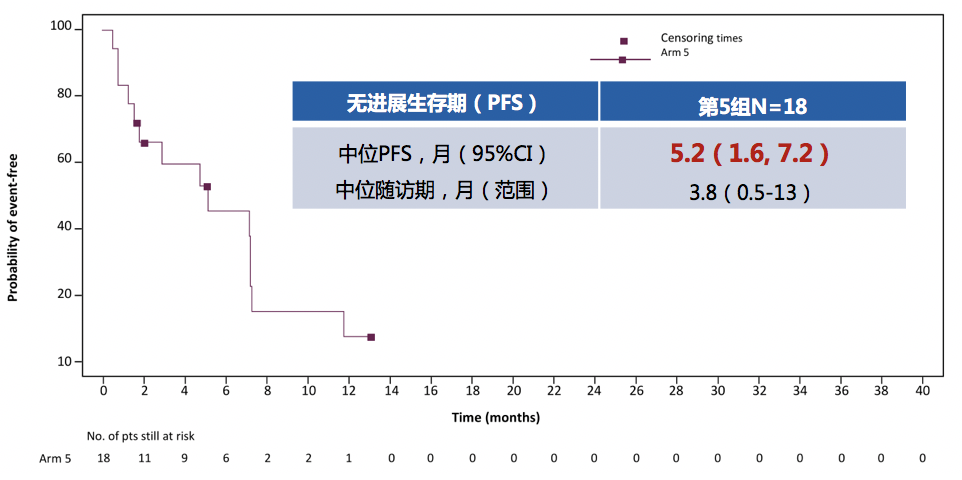
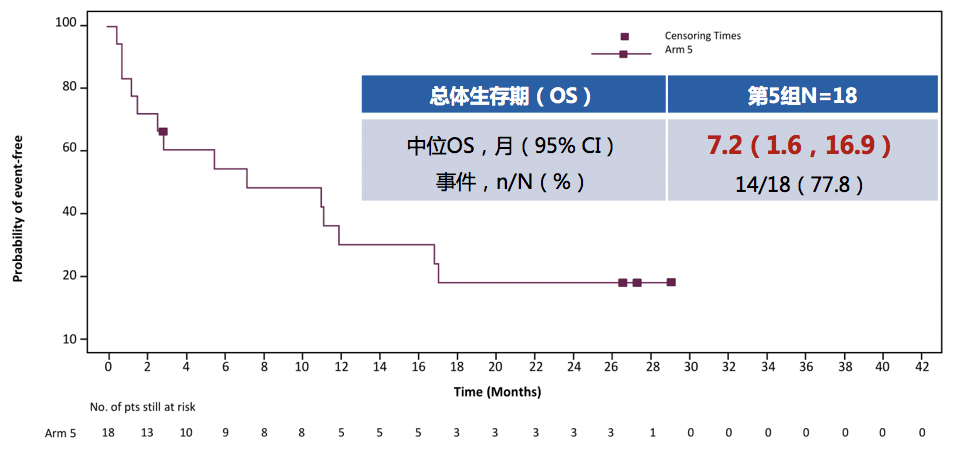 图4. ASCEND-7脑膜转移患者研究结果
图4. ASCEND-7脑膜转移患者研究结果
来源:Lancet Oncol. 2016;17(4):452-463. , J Clin Oncol 34:4079-4085
3. 全身控制
1)塞瑞替尼/阿来替尼vs.克唑替尼:塞瑞替尼与ALK靶点的亲和力是一代ALK抑制剂的20倍,是阿来替尼的12.7倍。ALEX研究显示,阿来替尼对全身病灶的控制与克唑替尼一致。一项台湾的回顾性研究结果显示,经塞瑞替尼治疗患者的全身病灶的控制显著优于克唑替尼组。
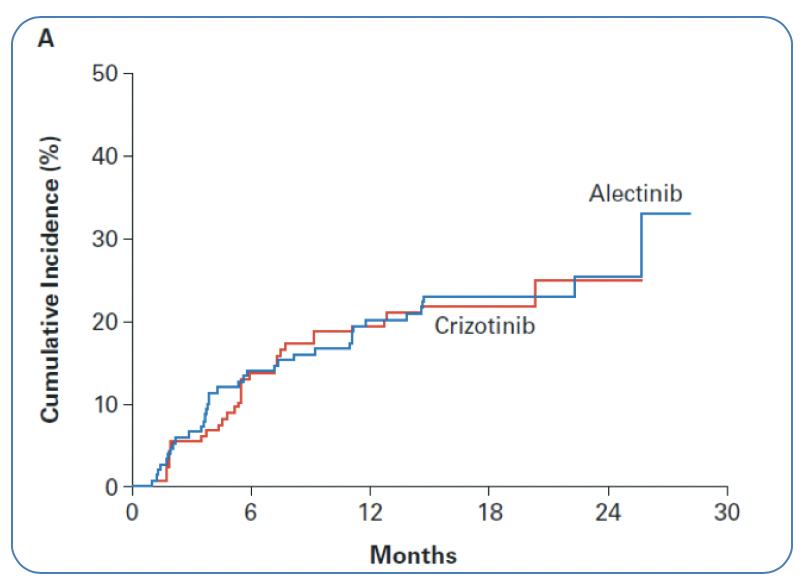
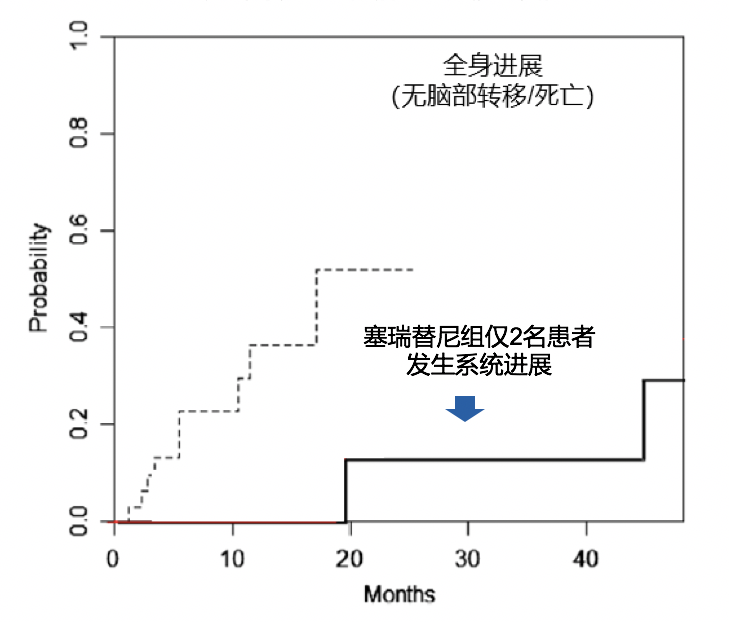
图5.阿来替尼/塞瑞替尼vs.克唑替尼对全身病灶的控制
来源:N Engl J Med 2017; 377:829-838;Thoracic Cancer ISSN 1759-7706
2)肝/骨/脑等远处转移病灶疗效
在一项美国回顾性研究中,一代克唑替尼耐药后采用塞瑞替尼治疗,对肝/骨/脑转移的ORR分别可达63.6%、74.1%、70.0%。
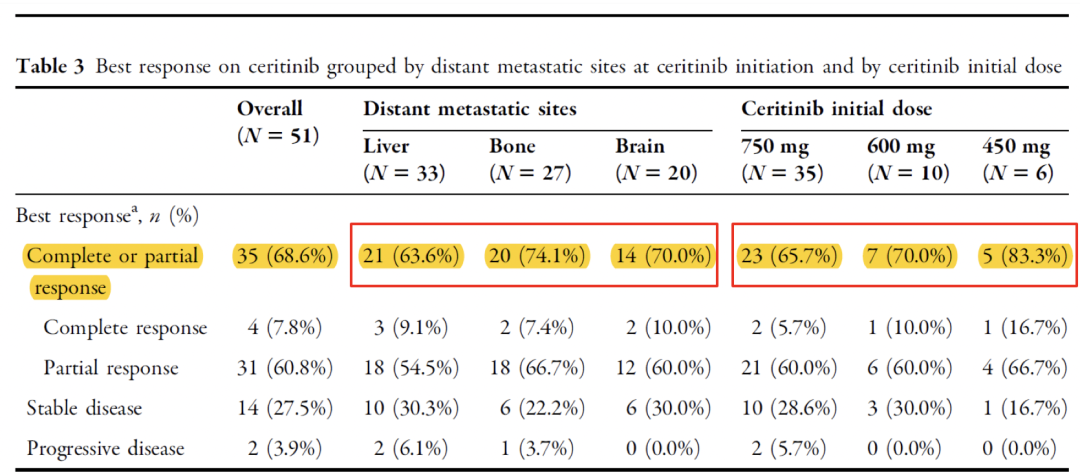 图6.阿来替尼/塞瑞替尼vs.克唑替尼对全身病灶的控制
图6.阿来替尼/塞瑞替尼vs.克唑替尼对全身病灶的控制
来源:Adv Ther (2017) 34:1145–1156
3. 耐药机制
克唑替尼常见两种耐药机制,一为中枢神经耐药,另一为系统性耐药,其中约1/3的复发患者存在ALK激酶结构域的继发性耐药突变, 1196/1171/1269突变高达60%,其他耐药机制包括ALK扩增/拷贝数增加、已知突变信号通路/旁路的激活(如EGFR, c-KIT, KRAS)等。研究显示,无论有无ALK二次突变位点,使用塞瑞替尼均有效,且塞瑞替尼对1196/1171/1269位点突变敏感。
?
1. 不同的临床研究入组人群基线都不同,这会对研究结果有多大影响?塞瑞替尼450mg随餐减量增效更安全,您认为在二线,这一剂量是否会带来更好的疗效?在临床实践中,如何看待不同的二代ALK抑制剂在克唑替尼耐药人群中的疗效和安全性?可否分享您的临床体验?
林根教授:不同临床研究中患者基线特征差异较大,因此不能简单地做不同药物间的直接比较,今后可通过大样本的真实世界研究来解答。
塞瑞替尼450mg减量增效的依据有以下三点。首先,塞瑞替尼在一定剂量范围下,都能达到有效浓度。其次,药代动力学参数显示,450mg剂量的AUC曲线下面积、峰浓度都可达到750mg剂量的水平,且患者耐受性好,依从性增高。最后,塞瑞替尼的半衰期较长,导致胃肠道副作用主要是由于对胃肠道的直接刺激,因此,个人认为甚至可以尝试小剂量分次服用的方法,减少胃肠道刺激,也可能会带来很好的疗效和安全性。
临床中,可根据NGS检测结果明确耐药机制,个体化选择相应的二代ALK抑制剂。
史健教授:二代ALK抑制剂塞瑞替尼和阿来替尼的临床研究中,入组人群存在差异,主要体现在前期治疗不同、基因检测的异质性和耐药的多样性,因此,研究结果有所差异。
塞瑞替尼450mg随餐剂量具有有效剂量小、毒副作用小、经济负担低的特点,因此,疗效更好,依从性更高,有利于临床应用和患者居家管理。
克唑替尼耐药后,建议行基因检测选择后续治疗。
姚煜教授:不同临床研究中入组患者的基线特征及预后因素不同,例如性别、PS评分等不同均会影响研究结果。
在ASCEND-8研究中,不同剂量塞瑞替尼(450mg、600mg、750ng)的Cmax、Tmax、AUC面积均高度一致,450mg随餐可达与750mg空腹相仿的血药浓度,但是胃肠道毒性明显下降、患者耐受性增加。
克唑替尼耐药后,也建议根据NGS检测针对性的选择用药。
2. 有症状,进展期的脑转移患者愈后和疗效都会更差,这与您在临床上的体会一致么?随着对研究基线数据的进一步挖掘,您如何评估塞瑞替尼在颅内病灶的疗效?
林根教授:以往对脑转移的预后评分系统是基于手术、放疗等治疗手段,如今靶向治疗、免疫治疗都体现出对脑转移的疗效。因此,对脑转移的评估入组标准可能需要相应改变。
塞瑞替尼的研究中与时俱进地纳入了有症状、进展期的脑转移患者,研究结果显示其对颅内病灶的良好疗效,提示塞瑞替尼不论是对有症状、无症状,还是脑膜转移或脑实质转移病灶,疗效都是相当不错的。
姚煜教授:临床中,有症状、进展期的脑转移患者,尤其是脑膜转移患者通常进展迅速、预后非常差。采用RECIST评价标准来评判脑转移疗效可能存在不足,脑转移患者的疗效影响因素较多,激素应用、症状控制等均会影响。
塞瑞替尼ASCEND-7研究中纳入了有症状、进展期的脑转移患者,研究结果显示其对脑转移病灶起效快,持续时间较长,期待后续中位OS的报道数据。
3. 您是否遇到过ALK阳性NSCLC脑膜转移的患者?从您的治疗经验来看,您认为对于这种比较棘手的患者,应该如何予以治疗?放疗在脑转移的治疗中有着重要的作用,您如何看待ALK抑制剂与放疗的关系?
董晓荣教授:ALK、EGFR驱动基因阳性NSCLC患者易出现脑转移,包括脑实质、脑膜转移两类,脑膜转移的预后明显差于脑实质转移,治疗棘手。脑转移是全身疾病的局部表现,因此应在控制全身性疾病的基础上加用局部治疗。早期的化疗药物难以进入颅内,疗效不理想,在目前分子靶向治疗时代,ALK/EGFR-TKI能较好的控制颅内病灶,其中二代ALK抑制剂疗效优于一代。对于ALK阳性脑转移患者,可采用ALK抑制剂同时加用局部治疗手段,例如放疗包括SRS、WBRT等。
姚煜教授:脑膜转移较脑实质转移病情更为凶险。ASCEND-7研究显示,脑膜转移组患者应用塞瑞替尼治疗后,ORR可达20%。ALK阳性NSCLC对放疗敏感,ALK阳性脑转移患者是选择同步放疗加ALK抑制剂抑或先放疗后用ALK抑制剂呢?在临床实践中,同步进行的情况更多些,但目前二三代ALK抑制剂上市,对于多发脑转移患者,先通过药物控制病情,推迟放疗也可能是不错的选择。总之,根据患者情况,在适当时机选择合适的治疗、多种手段结合能更好地延长患者生存。
史美祺教授:脑膜转移、脑实质转移的患者预后极差,在化疗时代通常采用脑部放疗控制,但在靶向治疗时候,对于ALK阳性脑转移患者,采用二三代ALK抑制剂可取得较好的疗效,因此,对放疗和靶向孰先孰后存在着争议。ALK阳性脑转移患者在能获得长生存的情况下,过早放疗面临着后续放疗脑损伤的问题,其治疗模式需要进一步探索。
4. 克唑替尼与阿来替尼的亲和力相近,导致两者对全身进展的控制能力相近,这与您的临床经验相一致么?塞瑞替尼针对全身不同转移灶都有很好的疗效,这与您的临床经验相一致么?您是否会根据不同的转移灶来选择治疗方案?
史健教授:克唑替尼和阿来替尼的亲和力相近。在临床中,对于无脑转移的患者,鉴于当地患者的经济条件,一线会选用克唑替尼,进展后根据基因检测结果选择用药。
转移病灶所涉及的脏器代偿能力不同,因此治疗的方法和原则可能不同。脑转移可能合并颅高压症状,需要尽快处理,应首选能通过血脑屏障的药物。脑膜转移属于不可测量病灶,可行脑脊液基因检测,若有合并基因突变,例如HER2突变,可加用曲妥珠单抗全身使用或腰椎穿刺鞘内注射。总之,真实世界中所遇到的患者情况多样,应个体化的分析治疗。
林根教授:比较靶向药物的疗效应以研究终点作为金标准,尽管克唑替尼与阿来替尼的亲和力相近,但在一线治疗中,阿来替尼比克唑替尼PFS延长、ORR更佳。
肝、骨、脑、肺、肾上腺等不同转移灶的微环境不同,对治疗反应可能存在异质性。临床治疗中,应先评估转移灶对生存或生活质量的影响程度。举例来说,脑膜转移患者因其预后差,往往需要进行较为强烈的干预措施,在一般情况良好的情况下,采用“重拳出击”、联合手段,例如免疫联合靶向、化疗,甚至加用抗血管生成药物,以及鞘内注射。
史美祺教授:靶向药物的量效关系并非线性,例如塞瑞替尼450mg对比750mg,反而是450mg疗效更好。因此,判断靶向药物的疗效差异还应依据研究终点,而非其他中间指标。
有关不同转移灶对治疗的异质性,需要积累更多临床研究结果来解答。不同转移病灶的治疗方案选择,若患者一般情况较好,可联合重拳出击,以期延长生命,若处于终末期、一般情况较差,则以减轻痛苦、提高生活质量为主要治疗目的。
姚煜教授:克唑替尼和阿来替尼的药物结构、分子设计不同,药代动力学参数有差异,临床实验的结果提示,阿来替尼的疗效包括PFS、ORR均优于克唑替尼。
不同转移病灶存在异质性,建议行再活检根据检测结果,例如ALK通路依赖或非ALK通路依赖的耐药机制来选择后续治疗。
5. 克唑替尼进展后,二次NGS测序是否是必须的?二次NGS测序的结果将如何指导下一步用药选择?
林根教授、史健教授、史美祺教授:克唑替尼耐药后,若患者经济条件允许,建议组织、血液NGS检测,根据结果精准选择后续药物。但是,克唑替尼耐药后的二次突变占比不高,尤其是对三代有效的G1202R耐药突变比例很低。因此,大多情况下选择二代ALK抑制剂都可取得不错的疗效。
1. 致死性不良反应、严重不良反应
致死性不良反应(AE)方面,阿来替尼和克唑替尼的发生率分别为4%和5%,塞瑞替尼(750mg空腹或450mg随餐)均未发生。
塞瑞替尼(450mg)和阿来替尼的严重不良反应(SAE)发生率分别为4.6%和36.0%,3-5级AE发生率分别为40.7%和49.0%,永久停药率分别为6.5%和14.0%。
2. 不同脏器的不良反应
肝脏方面,克唑替尼ALT、AST升高的比例高达79%和66%,阿来替尼胆红素升高比例高达53%,相比之下,塞瑞替尼对肝功能影响较低,在说明书中对肝功能的监测每月一次即可。
心脏方面,塞瑞替尼心动过缓发生率仅2.3%,克唑替尼为14%,阿来替尼11%。
间质性肺炎方面,克唑替尼和阿来替尼出现间质性肺炎的比例均为8%,塞瑞替尼发生率最低为2.1%。肾损伤方面,塞瑞替尼450mg随餐剂量下,肾脏AE发生率低于阿来替尼。
视力障碍、水肿、贫血方面,克唑替尼对眼部影响较大,塞瑞替尼在这方面安全性很好。
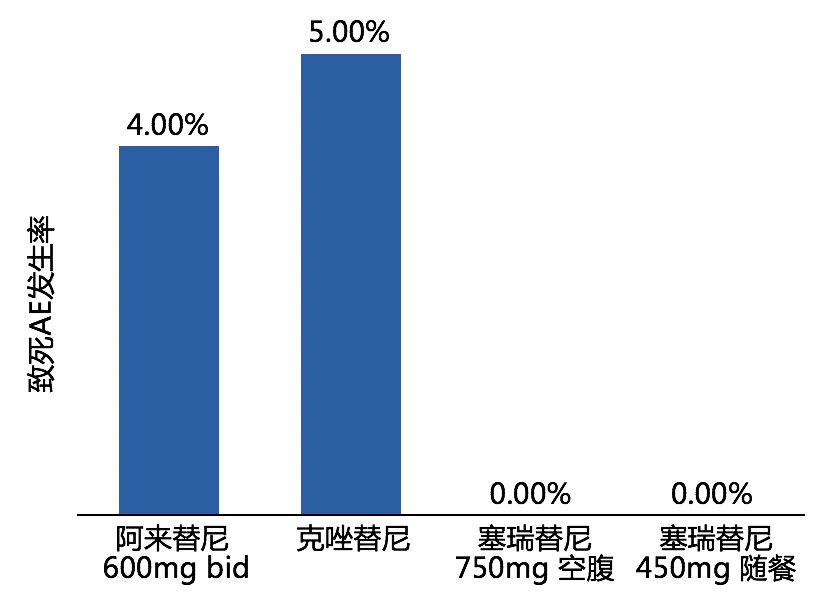
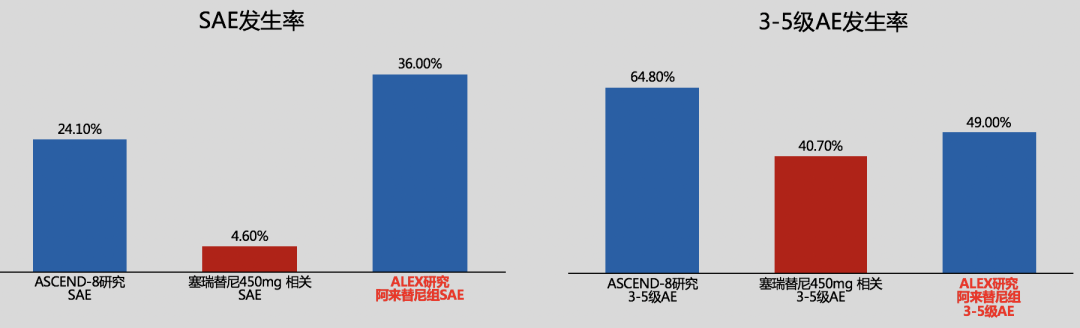
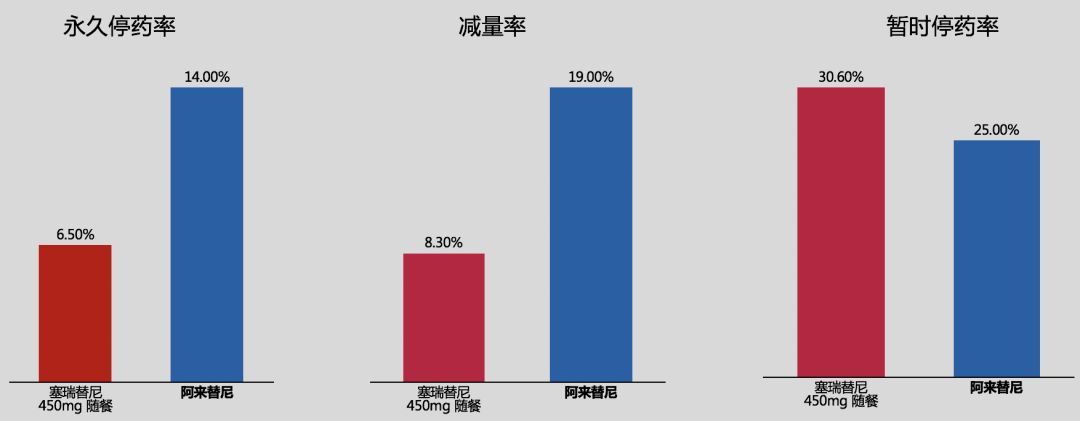
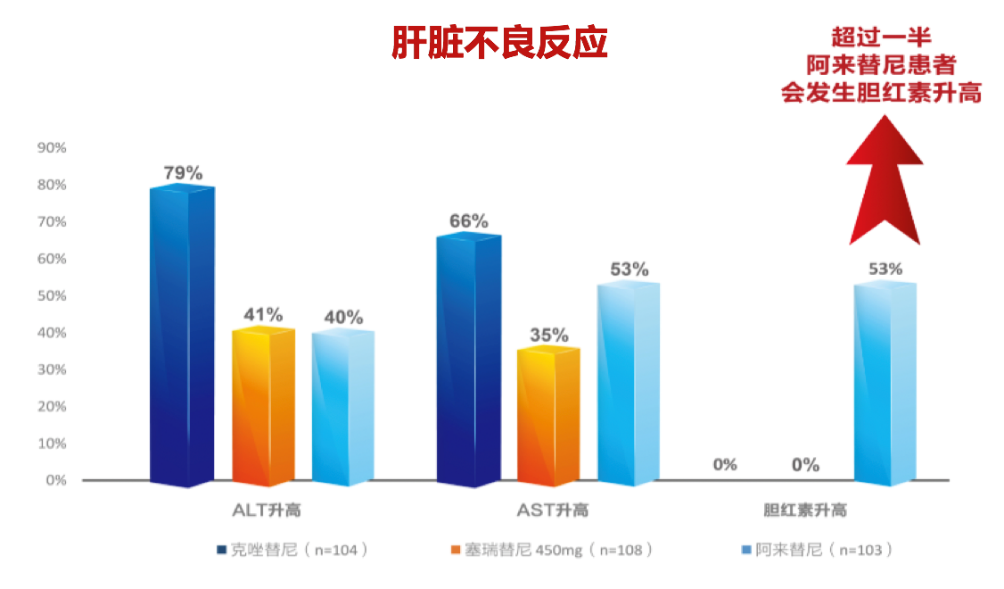
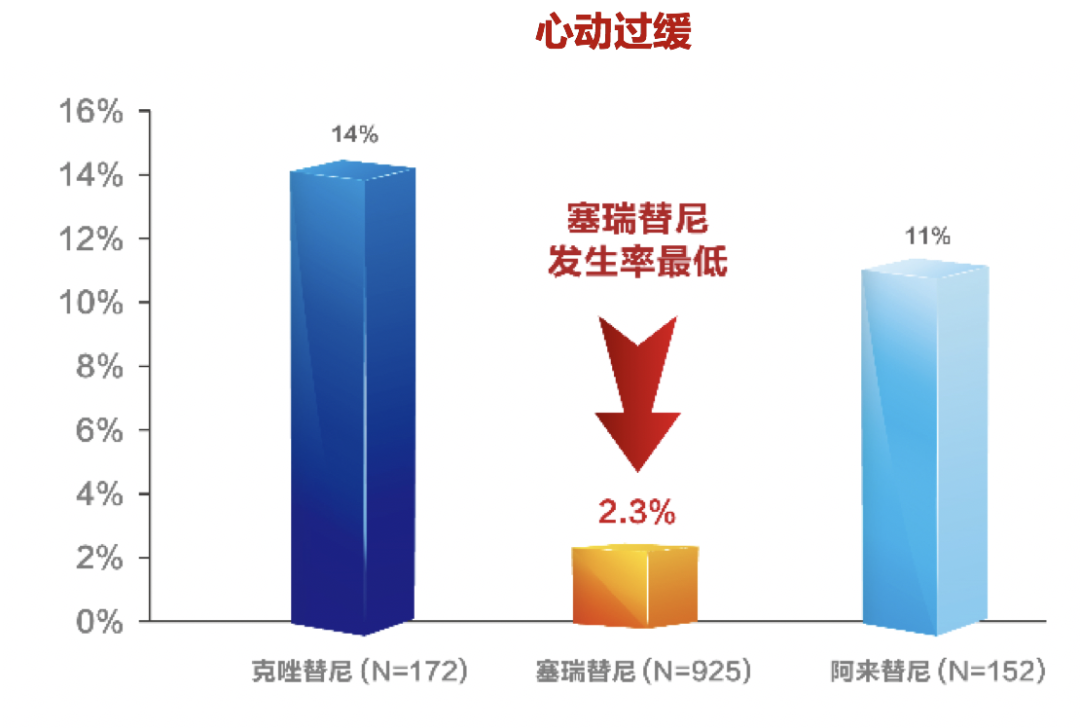
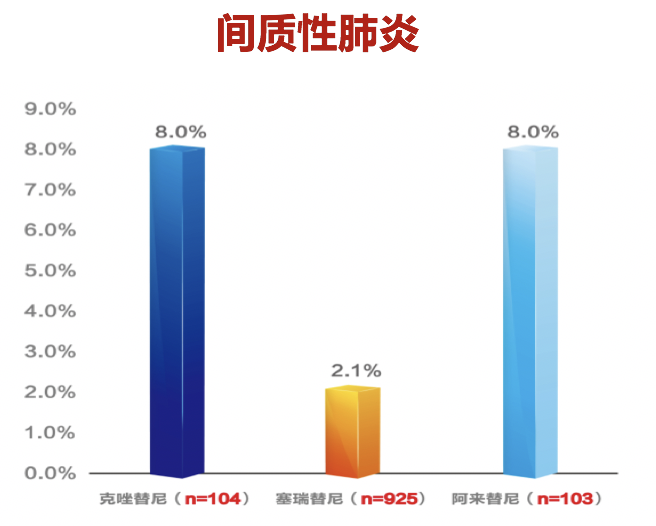
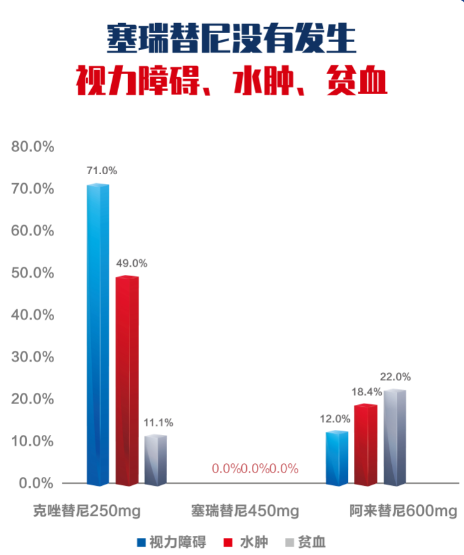 图7.克唑替尼/塞瑞替尼/阿来替尼不良反应来源:N Engl J Med 2017;377:829–38., J Thorac Oncol 2019;14:1233, Lancet. 2017;389(10072):917-929., ASCEND-8 LBA59; 2018 ESMO_Cho et_al; ALEX final PFS 1484PD; 2019 ESMO_Tony et_al
图7.克唑替尼/塞瑞替尼/阿来替尼不良反应来源:N Engl J Med 2017;377:829–38., J Thorac Oncol 2019;14:1233, Lancet. 2017;389(10072):917-929., ASCEND-8 LBA59; 2018 ESMO_Cho et_al; ALEX final PFS 1484PD; 2019 ESMO_Tony et_al
1. 在临床实践中,您对不同ALK抑制剂的使用感受是怎么样的?您认为治疗的依从性的提升对疗效重要么?在治疗初期,您会如何帮助患者提高治疗依从性?
董晓荣教授:ALK突变又称“钻石突变”,在临床实践中,ALK抑制剂的选择主要考虑三方面:总体疗效、特殊部位疗效和毒副反应。
总体疗效包括ORR、PFS和OS指标,已有研究结果显示,一代克唑耐药后序贯二代ALK抑制剂OS可长达89个月。特殊部位例如脑转移的疗效,要关注颅内iORR和iPFS等指标。不同ALK抑制剂的毒副反应不一,在疗效一致的情况下应选择毒副反应轻的药物,总体来说,二代药物毒副反应轻于一代。此外,应注意患者宣教,让患者知晓可能出现的毒副反应及应对措施。
史健教授:塞瑞替尼750mg临床研究中,较多患者因毒副反应导致停药或延迟治疗,450mg剂量AE明显减少。建议对存在高龄、合并症等高危因素的患者,若出现450mg剂量不可耐受的情况,可尝试首剂减量或在出现AE后减量,避免停药。
2. 在临床实践中,哪些不良反应对治疗的影响比较大?目前已有多个ALK抑制剂获批上市,且不良反应谱各有不同。您是否会结合药物的不良反应和患者的状态来选择药物?遇到哪些不良反应,您会考虑让患者换另一种药物治疗?
姚煜教授:鉴于不同ALK抑制剂AE谱的不同,对于特殊人群可做相应选择,例如有肝炎病史患者避免易引起肝损的克唑替尼,有毛细胆管炎的患者需注意阿来替尼引起的胆红素升高,既往有心动过缓或间质性肺病的患者,特别是老年患者,可选用在此方面安全性更高的塞瑞替尼,从而减低AE发生、提高患者依从性,有助于获得良好的疗效。
史健教授:出现肝损等AE,需要考虑药物和病灶的双重影响因素,建议肝脏胆管B超,评估局部治疗的可能性。此外,在口服靶向药物的居家管理中,要告知患者需要长期的动态评估。
林根教授:严重AE或致死性AE对治疗反应影响大。治疗前应全面评估患者分期、病理、基因、合并症等情况,根据不同药物AE谱的特征和患者具体情况,有针对性地选择药物,避免AE出现;若出现AE,应做减量、对症处理或换药治疗。
史美祺教授活动总结:今天的活动主要介绍了二代ALK抑制剂包括塞瑞替尼的临床研究疗效及安全性数据,尤其是脑转移等特殊部位的疗效。塞瑞替尼从750mg减量至450mg随餐后,安全性大为改观,疗效有所提升。ASCEND-7研究显示了塞瑞替尼对脑转移患者的良好疗效。
一代克唑替尼耐药后二次突变1196/1171/1269突变比例达60%,基础研究显示塞瑞替尼对这些位点的IC50较其他ALK抑制剂更低,具有临床实践参考意义。ASCEND-8研究显示了塞瑞替尼450mg随餐剂量一线治疗的良好疗效和安全性,期待最终结果的公布。





 京公网安备 11010502033352号
京公网安备 11010502033352号